在探索異種移植人體研究上,中國學者再度實現突破。
近日,廣州醫科大學附屬第一醫院何建行教授研究團隊在國際權威學術期刊《自然-醫學》在線發表論文,報告了世界首例將基因編輯豬肺移植到腦死亡人體內成功案例,移植肺維持通氣與氣體交換長達9天,期內未發生超急性排斥反應,同步病原學監測也未發現活躍感染,這項研究被國際上形容為“具有里程碑意義”。
開展以基因編輯豬為供體的異種器官移植技術,意在解決器官短缺問題,為臨床器官移植提供穩定、可控的供體來源。近年來,隨著基因工程技術的進步和新型免疫抑制藥物的開發,以豬來源器官為主的異種移植研究逐漸增多,但從科研真正走到臨床應用,還面臨哪些挑戰?
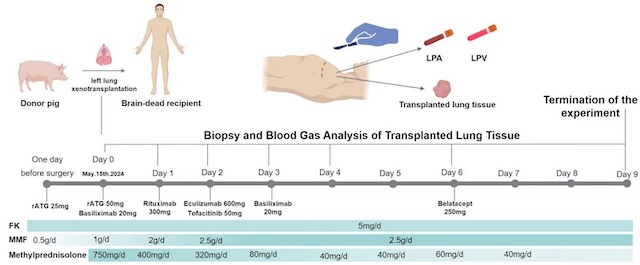
首例豬肺人體移植研究
這次基因編輯豬肺人體移植研究,是將一只經過基因編輯的巴馬香豬左肺移植到一名腦死亡者體內,模擬臨床常見的單肺移植手術,術后動態監測呼吸、血液、影像等多方面情況,持續評估排斥反應及感染情況。
該供體豬經過6處基因編輯,以降低其器官移植到人體后的免疫風險。
廣州醫科大學附屬第一醫院方面對第一財經記者表示,本次研究方案嚴格遵循國家有關法律法規和倫理準則,先后通過醫院倫理委員會等機構審查與監督。受試者為重型顱腦損傷患者,經多次獨立評估確認腦死亡;家屬出于支持醫學進步的愿望,同意無償參與科研。
文章通訊作者何建行表示,目前全球健康老齡化問題環境下,隨著器官移植技術的成熟,全球器官移植供體需求逐漸增大,異種器官移植被認為有望解決這一困境,該成果標志著異種肺移植領域邁出關鍵一步,接下來,將進一步優化基因編輯策略與抗排斥治療方案,延長移植器官存活時間及功能維持,并將團隊自主研發的無管技術應用于異種肺移植試驗中以減少機械通氣對供體肺的損傷,推動肺異種移植向臨床轉化。
云舟生物相關負責人對第一財經記者表示,這次豬肺人體移植,好比對豬肺做了一次“大改裝”,把可能讓人體“強烈過敏”的零件拆掉,再裝上“人類零件”以便兼容,再移植入一位腦死亡的患者中進行體內測試,移植后的前幾天,豬肺沒有出現最早期的“超急性排斥”,說明這樣的改造在往好的方向發展,但出現了水腫和抗體介導排斥,說明這種改造還不能完全消除異種排斥現象。與過去豬心、豬腎移植相比,這是全球首次豬肺進入人體,肺又是公認“最難”的器官,所以被認為具有里程碑意義。
該負責人表示,這次是在腦死亡患者上進行的研究,同時也保留了一邊人肺作為備用,但豬肺人體移植要走向臨床,還要解決功能驗證、長期穩定性、免疫抑制負擔、生物安全等問題。“簡單來講,這次試驗證明了豬肺‘能活’,但就像一個‘樣機’測試,離真正給活人應用還很遠。未來需要證明:豬肺能單獨支撐人體呼吸好幾周甚至幾個月,免疫抑制藥物的使用,不能多到讓人體完全失去免疫力,而且也不能帶來豬病毒風險。”
復旦大學上海醫學院副院長朱同玉對第一財經記者表示,這次國內開展的全球首例豬肺人體移植研究,是對不同豬來源器官移植又一次科研探索,可以進一步積累異體移植相關數據。
在此之前,中國科學院院士竇科峰帶領西京醫院等機構的研究團隊,以一只經過6處基因編輯的豬為供體,將豬的肝臟移植到一名已腦死亡但身體基本機能仍被維持的人體內,該研究今年3月份在線發表在《自然》雜志,也成為了世界首例將基因編輯豬的肝臟移植到腦死亡人體內的成功案例。
還有這些挑戰
隨著人類預期壽命的不斷延長,慢性病和終末期器官衰竭病人的數量日益增多,器官移植作為一種有效的治療手段,卻受限于供體器官的嚴重短缺。
世界衛生組織在《2023年全球器官移植觀察報告》中引述稱,目前中國每年約有30萬名患者等待器官移植,而可供移植的器官僅約1.5萬例,供需比例嚴重失衡。
異種移植是將動物源性的活細胞、組織、器官以移植、接種或注射的方式植入人體內的過程。異種器官移植作為國際生物醫學前沿技術,正成為緩解全球器官供需矛盾的重要突破口。
近幾十年來,異種移植研究在全球范圍內取得了一系列里程碑式的重大突破。2021年,有研究人員首次成功將基因編輯豬的腎臟移植到腦死亡患者體內,并存活了54小時。此后,研究者還在活體患者中成功進行了豬的心臟、腎臟和肝臟的移植實驗,其中心臟在人體內存活長達兩個月,這些進展為異種器官移植的臨床應用開辟了道路。
由于豬易于飼養繁殖,器官尺寸與人類較為匹配,遺傳學、生理學和解剖學方面與人類近似,被認為是最適合的異種移植供體,并可通過基因修飾來增強供體器官的匹配性。
前述云舟生物相關負責人表示,在異種器官移植上,基因編輯技術基本可以解決超急性排斥問題,說明改造豬器官能在某種程度上“騙過”人體免疫系統的第一波攻擊,但還沒有解決中長期排斥問題,比如抗體介導排斥和慢性排斥。另外,免疫抑制藥物還不夠安全,豬器官中的病毒風險也還沒徹底清除。
朱同玉表示,豬來源器官移植人體,目前還是處于科研階段,要真正走向臨床應用,還有很長路要走,其中的排斥反應仍然是一個不可逾越的障礙,術后存活時間相對長的患者,需要使用大量免疫抑制劑,患者本身很難忍受,而使用了大量免疫抑制劑后,又會產生感染問題,另外,可能還會出現豬和人共患病潛在風險。
朱同玉也是一名器官移植專家,他同時兼任上海市器官移植重點實驗室主任。這些年,他也在探索如何利用人工智能對動物器官進行基因編輯,從而進一步適應人體移植需要,但還在動物實驗階段,還未在人體上進行試驗。
朱同玉表示,從全球已開展的二十多例豬來源器官移植人體研究來看,術后最長的存活時間,大概半年多,相對臨床獲益有限。人體器官移植,術后平均生存期可以在十年以上。比如他經手的同種異體移植手術,有患者術后至今生存期超過40年。
“豬來源器官移植人體研究,仍需要進一步科學探索,從而尋找到更優化的組合方案。”朱同玉這樣認為。
竇科峰等人2025年1月在《中國實用外科雜志》發表的一篇關于《異種移植:從基礎到臨床的瓶頸與對策》研究中亦表示,要真正實現異種移植的臨床應用,仍需解決一系列關鍵問題,這些問題主要包括免疫排斥反應、生理兼容性問題、病原體跨物種傳播,以及倫理和法律問題。因此,盡管前景光明,異種移植在實現臨床轉化前仍有一段漫長的道路要走。
幫企客致力于為您提供最新最全的財經資訊,想了解更多行業動態,歡迎關注本站。鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播更多信息之目的,如作者信息標記有誤,請第一時間聯系我們修改或刪除,多謝。



